কানন পুরকায়স্থ
২০১৮ সালে পদার্থবিজ্ঞানে নোবেল পুরস্কার পেলেন যুক্তরাষ্ট্রের বেল ল্যাবরেটরিতে কর্মরত আর্থার এসকিন (Arthur Ashkin), ফ্রান্সের ইক্ল পলিটেকনিক এবং মিশিগান বিশ্ববিদ্যা
লয়ে কর্মরত জেরার্ড মোরু (Gerard Mourou) এবং কানাডার ওয়াটারলু বিশববিদ্যালয়ে কর্মরত ডনা স্ট্রিকল্যান্ড (Donna Strickland)। এসকিন ১৯২২ সালে যুক্তরাষ্ট্রের নিউইয়র্কে, মোরু ১৯৪৪ সালে ফ্রান্সের অ্যালবার্টভাইনে এবং স্ট্রিকল্যান্ড ১৯৫৯ সালে কানাডার গোয়েলপে জন্মগ্রহণ করেন। রাজকীয় সুইডিশ বিজ্ঞান অ্যাকাডেমি তাদের ২ অক্টোবর ২০১৮ সালের প্রেস রিলিজে উলেস্নখ করে যে, ‘For grand breaking intentions in the field of laser physics’-এর জন্য এই তিন পদার্থবিজ্ঞানীকে নোবেল পুরস্কার প্রদান করা হয়। পুরস্কারের অর্ধেক অর্থ অর্থাৎ ৪.৫ মিলিয়ন সুইডিশ ক্রোনা পান আর্থার এসকিন এবং বাকি অর্ধেক মোরু ও স্ট্রিকল্যান্ডকে সমানভাবে ভাগ করে দেওয়া হয়।
এ-বছর রসায়নবিজ্ঞানে নোবেল পুরস্কার পেলেন যুক্তরাষ্ট্রের ক্যালিফোর্নিয়া ইনস্টিটিউট অব টেকনোলজির লিনাস পলিং অধ্যাপক ফ্রান্সেস এইচ. আরনল্ড (Frances H. Arnold), যুক্তরাষ্ট্রের মিসৌরি বিশ্ববিদ্যালয়ের অধ্যাপক (এমেরিটাস) জর্জ পি. স্মিথ (George
P. Smith) এবং ইংল্যান্ডের এমআরসি ল্যাবরেটরি অব মলিকিউলার বায়োলজির রিসার্চ লিডার (এমেরিটাস) গ্রেগরি পি. উইন্টার। আরনল্ড ১৯৫৬ সালে যুক্তরাষ্ট্রের পিটসবার্গে, স্মিথ ১৯৪১ সালে যুক্তরাষ্ট্রের নোরওয়াকে এবং উইন্টার ১৯৫১ সালে ইংল্যান্ডের লেস্টারে জন্মগ্রহণ করেন। রাজকীয় সুইডিশ বিজ্ঞান অ্যাকাডেমি ৩ অক্টোবর ২০১৮ সালের প্রেস রিলিজে উলেস্নখ করে, ‘For the directed evolution of enzymes’ আবিষ্কারের জন্য ফ্রান্সেস আরনল্ডকে এবং ‘For the phage display of peptides and antibodies’ আবিষ্কারের জন্য জর্জ স্মিথ এবং গ্রেগরি উইন্টারকে রসায়নবিজ্ঞানে নোবেল পুরস্কার প্রদান করা হয়। পুরস্কারের অর্ধেক অর্থ অর্থাৎ ৪.৫ মিলিয়ন সুইডিশ ক্রোনা পান আরনল্ড এবং বাকি অর্ধেক অর্থ সমানভাবে বন্টন করে দেওয়া হয় স্মিথ ও উইন্টারের মধ্যে।
২০১৮ সালের জন্য শারীরবৃত্ত বা চিকিৎসাবিজ্ঞানে নোবেল পুরস্কার পেলেন যুক্তরাষ্ট্রের টেক্সাস বিশ্ববিদ্যালয়ের অধ্যাপক জেমস পি. এলিসন (James P. Allison) এবং জাপানের কিয়োটো বিশ্ববিদ্যালয়ের অধ্যাপক টাসুকু হোনজো (Tasuku Honjo)। জেমস এলিসন ১৯৪৮ সালে যুক্তরাষ্ট্রের টেক্সাসে জন্মগ্রহণ করেন। টাসুকু হোনজো ১৯৪২ সালে জাপানের কিয়োটো শহরে জন্মগ্রহণ করেন। সুইডেনের ক্যারোলিনস্কা ইনস্টিটিউটের নোবেল অ্যাসেম্বলি তাদের ১ অক্টোবর ২০১৮ সালের প্রেস রিলিজে উলেস্নখ করে, ‘For their discovery of cancer therapy by inhibition of negative immune regulation’-এর জন্য এলিসন এবং হোনজো নোবেল পুরস্কার পান। পুরস্কারের ৯.৫ মিলিয়ন সুইডিশ ক্রোনা এই দুই বিজ্ঞানীর মধ্যে সমানভাবে বণ্টন করে দেওয়া হয়। এই প্রবন্ধে উপরোলিস্নখিত নোবেল পুরস্কার-স্বীকৃত গবেষণার ওপর বিশদ আলোকপাত করব।
পদার্থবিজ্ঞান
আলো চাপ প্রয়োগ করার ক্ষমতা রাখে। আলোর এই কর্ম ১৬১৯ সালে রোহান কেপলার প্রথম উলেস্নখ করেন। কেপলারের একটি স্বীকার্য এই যে, একটি ধূমকেতুর পশ্চাৎভাগ সবসময় সূর্যের উলটো দিকে থাকে এবং এর কারণ হচ্ছে আলোর চাপ সৃষ্টি করার ক্ষমতা। ১৮৭৩ সালে বিজ্ঞানী জেমস ক্লার্ক ম্যাক্সওয়েল তাঁর তড়িৎচৌম্বকীয় তত্ত্বের মাধ্যমে তাত্ত্বিকভাবে দেখান যে, আলো চাপ প্রয়োগ করতে পারে। বিংশ শতাব্দীর গোড়ার দিকে লেবেদভ, নিকলস্ এবং গর্ডন হাল পরীক্ষার মাধ্যমে প্রমাণ করেন বিকিরণ চাপের অস্তিত্ব। ষাটের দশকের গোড়ার দিকে লেজার প্রযুক্তি আবিষ্কার হলো। এই লেজার হলো light amplification by stimulated emission of radiation (laser)। লেজার-রশ্মির সঙ্গে আলোকরশ্মির পার্থক্য এই যে,
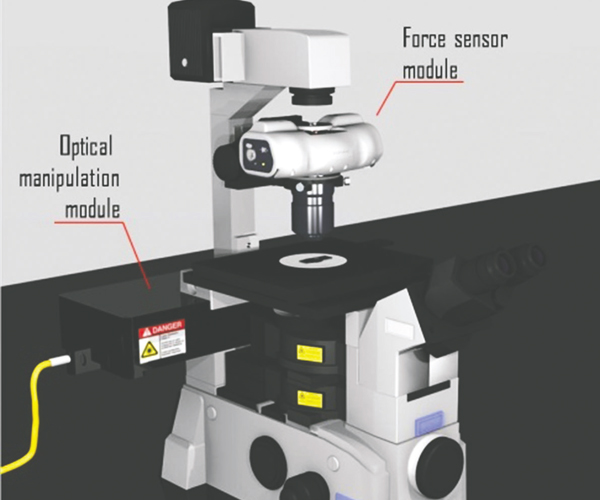
লেজার-রশ্মির সংসক্ততা (coherent) কম। অর্থাৎ লেজার আলো অত্যন্ত কেন্দ্রীভূতভাবে নিঃসৃত হয়। আর্থার এসকিন ১৯৭০ সালে দেখান যে, লেজার-রশ্মি থেকে আলোকীয় বল তৈরি হয় এবং তা দ্বারা ক্ষুদ্র ডাই-ইলেকট্রিক কণাকে তরল এবং বায়বীয় মাধ্যমে সরানো যায়। এসকিন লক্ষ করেন যে, লেজার-রশ্মি যে-চাপ কোনো কণার ওপর প্রয়োগ করে, তা ওই রশ্মির কেন্দ্রে সবচেয়ে বেশি। তাই এসকিন বিকীর্ণ রশ্মির মধ্যে একটি শক্তিশালী লেন্স বসান, যার ফলে রশ্মি আরো কেন্দ্রীভূত হয় এবং কোনো কণাকে রশ্মির কেন্দ্রের দিকে টেনে আনে অর্থাৎ আলোর তীব্রতা যেখানে বেশি, সেখানেই কণাগুলোকে ধরে রাখা যায়। এভাবেই এক ধরনের আলোর ফাঁদ (light trap) তৈরি করা সম্ভব হলো। অনেকটা সন্না বা চিমটার মতো কাজ করে বলেই এই পদ্ধতির নাম আলোকীয় সন্না বা optical tweezer যন্ত্র। একটি আলোকীয় সন্নার দৃশ্য চিত্র-১ দ্রষ্টব্য। এই যন্ত্র কেন্দ্রীভূত লেজার রশ্মির মাধ্যমে আকর্ষী বা বিকর্ষী বল তৈরি করে। এই বলের ধরন নির্ভর করে কোনো কণার প্রতিসরাংকের ওপর। এসকিন এই যন্ত্র ব্যবহার করে কণা, পরমাণু, ভাইরাস এবং অন্যান্য প্রাণিজ কোষকে ধরতে সমর্থ হন। এসকিন ভাবতে থাকেন কীভাবে জীবন্ত ব্যাকটেরিয়াকে তাদের কোনো ক্ষতিসাধন ছাড়া ধরা যায়।
তিনি লক্ষ করেন, লেজার-রশ্মি ব্যাকটেরিয়াকে ধ্বংস করে। তাই দুর্বল আলোকরশ্মির প্রয়োজন। তিনি ব্যবহার করেন অবলোহিত রশ্মি। তাতে জীবন্ত ব্যাকটেরিয়া কোনো ক্ষতি সাধন ছাড়াই ধরা সম্ভব। তিনি এই পদ্ধতির মাধ্যমে দেখান যে, কোনো কোনো ঝিলিস্নকে ধ্বংস না করেই কোষের অভ্যন্তরে প্রবেশ করা সম্ভব। তাঁর এই পদ্ধতি বিজ্ঞানের জগতে এক নতুন দিগমেত্মর উন্মোচন করল।
কোনো কোষের অভ্যন্তরে একটি অণু কীভাবে কাজ করে, তা এসকিনের এই পদ্ধতিকে কাজে লাগিয়ে জানা যায়। এই পদ্ধতি ব্যবহার করে বিভিন্ন জীবতন্ত্রে কোনো বস্ত্তকে স্পর্শ না করে তার সম্পর্কে অনুসন্ধান করা সম্ভব হয়েছে। অতিসম্প্রতি অপটিক্যাল হলোগ্রাফি পদ্ধতিতে অসংখ্য আলোকীয় সন্না ব্যবহার করা হচ্ছে এবং এর মাধ্যমে সুস্থ রক্তকোষকে সংক্রামিত কোষ থেকে পৃথক করা সম্ভব হচ্ছে। ম্যালেরিয়া রোগ প্রতিরোধের ক্ষেত্রে এই পদ্ধতি ব্যবহার করার চিন্তাভাবনা চলছে।
অন্যদিকে পদার্থবিজ্ঞানে নোবেল বিজয়ী জেরার্ড মোরু এবং ডনা স্ট্রিকল্যান্ড অতি হ্রস্ব এবং তীব্র লেজার স্পন্দন তৈরির পদ্ধতি আবিষ্কার করেন। তাঁদের এই পদ্ধতির নাম Chirped pulse amplification বা সিপিএ পদ্ধতি (চিত্র-২ দ্রষ্টব্য)। এই পদ্ধতি অনুযায়ী অতি হ্রস্ব লেজার স্পন্দনকে সম্প্রসারণ করা হয় পিটাওয়াট পর্যন্ত। এখানে ওয়াট হচ্ছে শক্তির একক। এক ওয়াট মানে হচ্ছে প্রতি সেকেন্ডে এক জুল শক্তি। পিটাওয়াট হচ্ছে ১০১৫ ওয়াট। এই সম্প্রসারণ প্রক্রিয়া কোনো বস্ত্তর ক্ষতিসাধন না করে করা হয়। যখন স্পন্দনকে সম্প্রসারণ করা হয়, তখন স্পন্দনচূড়ার ক্ষমতা কমে যায়। তারপর লেজার স্পন্দনকে সংকুচিত করা হয়। এই সংকোচনের ফলে অধিক পরিমাণ আলো কম স্থানে আবদ্ধ হয়। এতে স্পন্দনের তীব্রতা বেড়ে যায়। এভাবেই অতি হ্রস্ব এবং তীব্র লেজার স্পন্দন তৈরি করা হয়।
সিপিএ পদ্ধতি ষাটের দশকে রাডারের ক্ষমতা বাড়ানোর কাজে ব্যবহার করা হয়। মোরু এবং স্ট্রিকল্যান্ড আশির দশকে এই পদ্ধতির উন্নতিসাধন করেন। এই পদ্ধতিকে চোখের অস্ত্রোপচারের কাজে ব্যবহার করা হয়। একটি বৈদ্যুতিক অন্তরককে (insulator) এই পদ্ধতি দ্বারা বিদ্যুৎপরিবাহী পদার্থে রূপান্তর করা যায়। বিভিন্ন পদার্থের মধ্যে গর্ত সৃষ্টি করা বা যে-কোনো পদার্থ অত্যন্ত সূক্ষ্মভাবে কাটার কাজে সিপিএ পদ্ধতি ব্যবহার করা হয়ে থাকে। এই কৌশল ব্যবহার করে ডাটা সংরক্ষণের নতুন পদ্ধতি আবিষ্কার করা হয়েছে। সাম্প্রতিক কালে মোরু এবং স্ট্রিকল্যান্ডের পদ্ধতি ব্যবহার করে শুরু হয়েছে এটো সেকেন্ড পদার্থবিজ্ঞানে। এটো সেকেন্ড মানে হচ্ছে ১০-১৮ সেকেন্ড। এই পদ্ধতির সাহায্যে কোনো পরমাণুতে ইলেকট্রনের গতিবিধি পর্যবেক্ষণ এবং নিয়ন্ত্রণ করা সম্ভব। তাছাড়া মানবদেহে ক্যান্সার কোষকে নির্মূল করার জন্য এই পদ্ধতির ব্যবহার এখন বিজ্ঞানীরা পরীক্ষা-নিরীক্ষা করে দেখছেন। গত ৮ ডিসেম্বর ২০১৮ সালে স্টকহোম বিশ্ববিদ্যালয়ে নোবেল পুরস্কার সংক্রান্ত ভাষণে ডনা স্ট্রিকল্যান্ড উলেস্নখ করেন, তাঁর পিএইচ. ডি সুপারভাইজার জেরার্ড মোরু স্বপ্ন দেখিয়েছিলেন এই সিপিএ পদ্ধতির। তিনি সেই স্বপ্নের বাস্তবায়ন করেছেন। স্ট্রিকল্যান্ড উলেস্নখ করেন যে, এই কাজটি শুরু হয়েছিল তাত্ত্বিক পদার্থবিজ্ঞানী মারিয়া মেয়ারের (Maria Goeppert Mayer) হাতে। মেয়ার প্রথম উলেস্নখ করেন যে, একটি পরমাণু অনেক ফোটন কণাকে একই সময়ে শোষণ করতে পারে। এই তত্ত্বটি স্ট্রিকল্যান্ড তাঁর পিএইচ. ডি থিসিসে উলেস্নখ করেন।
রসায়নবিজ্ঞান
চিরাচরিত রসায়নবিজ্ঞানে রাসায়নিক দ্রবণ ব্যবহার করে বিভিন্ন রাসায়নিক পদার্থ তৈরি করা হয়। বিষয়টি বিজ্ঞানী ফ্রান্সেস আরনল্ড চিন্তা করলেন অন্যভাবে। এনজাইম বিভিন্ন জীবাণুতে সংঘটিত রাসায়নিক বিক্রিয়ায় প্রভাবক হিসেবে কাজ করে। সুতরাং নতুন এনজাইম যদি তৈরি করা যায়, তাহলে তাকে ব্যবহার করে নতুন নতুন রাসায়নিক পদার্থ তৈরি করা সম্ভব। একটি এনজাইম কয়েক হাজার অ্যামিনো অ্যাসিড দ্বারা গঠিত। সুতরাং নতুন এনজাইম তৈরি অত্যন্ত জটিল কাজ। আরনল্ড ভাবলোবাসেন, প্রাকৃতিকভাবে যে-বিবর্তন ঘটে, সেই বিবর্তনকে রসায়নবিজ্ঞানের কাজে কীভাবে ব্যবহার করা যায়। আরনল্ড ‘সাবটিলিসিন’ (subtilisin) নামক এক ধরনের এনজাইম নিয়ে কাজ শুরু করেন। তিনি সেই এনজাইমের জেনেটিক কোডে পরিব্যক্তি (mutation) ঘটান। তারপর এই পরিব্যক্ত জিনকে ব্যাকটেরিয়ার মধ্যে প্রয়োগ করা হয় এবং তা থেকে তৈরি হয় সাবটিলিসিন অণুর এক অসমরূপ (variant)। এর পরের ধাপ হচ্ছে কোন অসম সাবটিলিসিন জৈব দ্রবণে ভালোভাবে কাজ করে তা খুঁজে বের করা। বিবর্তনের ক্ষেত্রে আমরা ‘Survival of the fittest’ কথাটি ব্যবহার করি, কিন্তু নির্দেশিত বিবর্তনের ক্ষেত্রে এই ধারাকে বলা হয় ‘নির্বাচন’। সাবটিলিসিন দুধে বিদ্যমান প্রোটিন অণু কেসিনকে ভাঙতে পারে। আরনল্ড সাবটিলিসিন অণুর একটি অসমরূপকে নির্বাচন করেন যেটি কেসিন অণুকে
ডাই-মিথাইল ফরমামাইডের দ্রবণে অত্যন্ত কার্যকরভাবে ভাঙতে পারে। আরনল্ড পুনরায় সাবটিলিসিনের জেনেটিক কোডে পরিব্যক্তি ঘটান এবং তা থেকে প্রাপ্ত সাবটিলিসিনের নতুন অসম রূপ ডাই-মিথাইল ফরমামাইড দ্রবণে আরো বেশি কার্যকর হয়। এভাবেই এনজাইমের নির্দেশিত, বিবর্তন বা directed evolution-কে কাজে লাগিয়ে ফ্রান্সেস আরনল্ড রসায়নবিজ্ঞানের জগতে নতুন নতুন যৌগ সৃষ্টির এক পদ্ধতি আবিষ্কার করেন, যার মূলনীতি ডারউইনের বিবর্তনবাদের ধারণার ওপর ভিত্তি করে প্রতিষ্ঠিত হয়। (আরনল্ডের ‘নির্দেশিত বিবর্তন পদ্ধতি’র বিভিন্ন ধাপ চিত্র-৩ দ্রষ্টব্য।) এই পদ্ধতি এখন প্রোটিন ইঞ্জিনিয়ারিংয়ে ব্যবহার করা হয়।
১৯৯৩ সালে আরনল্ড এনজাইমের প্রথম নির্দেশিত বিবর্তন ঘটান, যা রাসায়নিক বিক্রিয়ায় প্রভাবক হিসেবে কাজ করে। আরনল্ড উলেস্নখ করেন যে, ‘নির্দেশিত বিবর্তনের মাধ্যমে পরীক্ষাগারে একটি নতুন মাত্রা যুক্ত হলো। এই পদ্ধতির মাধ্যমে এনজাইমের বিবর্তনকে প্রভাবক হিসেবে বিভিন্ন বাণিজ্যিকভাবে কার্যকর রাসায়নিক বিক্রিয়ায় প্রয়োগ করা সম্ভব হলো।’
অপরদিকে জর্জ স্মিথ এবং গ্রেগরি উইন্টারের মূল কাজ হলো পেপটাইড এবং অ্যান্টিবডির জীবাণু ভাইরাস প্রদর্শনের পদ্ধতি আবিষ্কার। ১৯৮৫ সালে স্মিথ জীবাণু ভাইরাস প্রদর্শন (phage display) পদ্ধতি আবিষ্কার করেন। এই পদ্ধতি অনুযায়ী ভাইরাস ব্যাকটেরিয়াকে সংক্রমিত করে এবং তার মধ্যে তৈরি হয় নতুন প্রোটিন। বস্ত্তত ভাইরাস দ্বারা ব্যাকটেরিয়াকে ধ্বংস করার মাধ্যমে নতুন প্রোটিন তৈরি করা হয়। এই পদ্ধতি ব্যবহার করে উইন্টার অ্যান্টিবডির নির্দেশিত বিবর্তন ঘটান। উইন্টারের উদ্দেশ্য হচ্ছে নতুন ভেষজ তৈরি করা। এই পদ্ধতি অনুযায়ী প্রথম যে-ওষুধ তৈরি করা হয় তার নাম এডালিমুমেব (adalimumab)। এই ওষুধ বাত ও সন্ধিপ্রদাহ রোগের ক্ষেত্রে ব্যবহার করা হয়। সম্প্রতি এই পদ্ধতির মাধ্যমে আরো নতুন অ্যান্টিবডি তৈরি করা সম্ভব হয়েছে, যা রোগ স্থানান্তর সংক্রান্ত ক্যান্সার (Metastatic cancer) নিরাময় করে।
গত ৮ ডিসেম্বর ২০১৮ সালে স্টকহোম বিশ্ববিদ্যালয়ে নোবেল পুরস্কার সংক্রান্ত সম্ভোজন বক্তৃতায় ফ্রান্সেস আরনল্ড উলেস্নখ করেন যে, নিউটনের আপেল মাটিতে পড়ে কেন – এই প্রশ্নের উত্তরে একজন পদার্থবিদ বলবেন মাধ্যাকর্ষণ বলের কারণে তা সম্ভব হয়, যে-বল দুটি বস্ত্তর ওপর এমনভাবে কাজ করে যে যার মান দুটি বস্ত্তর ভরের গুণফলের সমানুপাতিক এবং দুটি বস্ত্তর দূরত্বের বর্গের বিপরীত আনুপাতিক। অপরদিকে একদল বিবর্তনবাদী জীববিদ এই প্রশ্নের উত্তরে বলবেন যে, একসময় আপেল ভূপৃষ্ঠে পড়ে থাকত। তাদের মধ্য থেকে যে সমস্ত আপেল অঙ্কুরিত হয়েছিল, তারাই বৃক্ষক্ষ পরিণত হয় এবং বিবর্তনের বলের কারণেই আপেল মাটিতে পড়ে। আরনল্ড উলেস্নখ করেন যে, ‘আমরা এই তিন রসায়নবিদ পদার্থ ও জীববিজ্ঞানের ধারণাকে কাজে লাগিয়ে নতুন অণু তৈরি করার কাজ করেছি, যা মানুষের কল্যাণে ব্যবহৃত হচ্ছে।’ নির্দেশিত বিবর্তন পদ্ধতি প্রয়োগ এবং জীবাণু ভাইরাস প্রদর্শন পদ্ধতি ব্যবহার করে এখন
পৃথিবীর বিভিন্ন দেশে নতুন নতুন পরিবেশবান্ধব রাসায়নিক যৌগ, জৈব জ্বালানি এবং জীবন রক্ষাকারী ওষুধ তৈরি করা সম্ভব হয়েছে।’
চিকিৎসাবিজ্ঞান বা শারীরবৃত্ত
ক্যান্সার রোগ বিভিন্ন ধরনের রোগের সমষ্টি হতে পারে, কিন্তু ক্যান্সার রোগের বিশেষ লক্ষণ হচ্ছে অস্বভাবী কোষের অনিয়ন্ত্রিত বৃদ্ধি এবং সুস্থ কোষকলার মধ্যে তা ছড়িয়ে পড়ার ক্ষমতা। এ-যাবৎ ক্যান্সারের বিভিন্ন ধরনের চিকিৎসাপদ্ধতির মধ্যে রয়েছে সার্জারি, বিকিরণ,
কেমোথেরাপি, হরমোন চিকিৎসা এবং অস্থিমজ্জা প্রতিরোপণ পদ্ধতি। বিংশ শতাব্দীর শুরুর দিকে ধারণা করা হয় যে, আমাদের দেহের অনাক্রম্য (immune) পদ্ধতিকে সক্রিয়করণের মাধ্যমে ক্যান্সার রোগকে প্রতিরোধ করার বিষয়টি একটি কৌশল হতে পারে। মানবদেহের অনাক্রম্যতা পদ্ধতির একটি মৌলিক ধর্ম হচ্ছে বিভিন্ন অনাকাঙিক্ষত জীবাণুর হাত থেকে দেহকে রক্ষা করা। এখানে উলেস্নখ্য, আমাদের দেহের শ্বেত রক্তকোষের একটি ধরন হচ্ছে লসিকা কোষ (Lymphocyte)। এই কোষের কেন্দ্রে রয়েছে কোষপ্রাণ (Cytoplasm)। আমাদের দেহে এক লিটার রক্তের মধ্যে
১.৫-৪ x ১০৯-টি লসিকা কোষ আছে। এই কোষ অনাক্রম্য কোষ হিসেবে কাজ করে। এই কোষ দুই ধরনের – ‘বি’ লসিকা কোষ (B-cell) এবং ‘টি’ লসিকা কোষ (T-cell)। ‘বি’ লসিকা কোষ অ্যান্টিবডি তৈরি করে এবং ‘টি’ লসিকা কোষ কোষমাধ্যমে অনাক্রম্যতার জন্য কাজ করে।
নববইয়ের দশকে ক্যালিফোর্নিয়া বিশ্ববিদ্যালয়ে ‘টি’ কোষ প্রোটিন CTLA-4 নিয়ে কাজ করার সময় জেমস এলিসন লক্ষ করেন যে, CTLA-4 ‘টি’ কোষের গতিরোধক বা ব্রেকের মতো কাজ করে। এলিসন একটি অ্যান্টিবডি তৈরি করেন, যা
CTLA-4-এর সঙ্গে বন্ধন তৈরি করতে এবং তার কার্যকারিতাকে রোধ করতে পারে। তারপর তিনি পরীক্ষা-নিরীক্ষা করে দেখেন যে, এই গতিরোধের ফলে ‘টি’ কোষের অনাক্রম্যতা পদ্ধতি সক্রিয় হয় এবং ক্যান্সার কোষকে ধ্বংস করে। ১৯৯৪ সালে এলিসন এবং তাঁর সহকর্মী ক্যান্সার রোগে আক্রান্ত ইঁদুরের ওপর অ্যান্টিবডি প্রয়োগ করেন এবং লক্ষ করেন যে, অ্যান্টিবডি কোষের গতিরোধ করা থেকে শুরু করে ‘টি’ কোষ কর্তৃক ক্যান্সার কোষকে ধ্বংস করার ক্ষমতা বৃদ্ধি পায়। ২০১০ সালে এই পদ্ধতিকে কাজে লাগিয়ে ত্বকের ক্যান্সার নিরাময় করা সম্ভব হয়।
এদিকে ১৯৯২ সালে জাপানের কিয়োটো বিশ্ববিদ্যালয়ের গবেষক টাসুকু হোনজো PD-1 নামে একটি প্রোটিন আবিষ্কার করেন। তিনি লক্ষ করেন যে, PD-1, CTLA-4-এর মতোই ‘টি’ কোষে গতিরোধক হিসেবে কাজ করে। কিন্তু এর কলাকৌশল একটু ভিন্ন ধরনের। ক্যান্সার নিরাময়ের ক্ষেত্রে PD-1-কে লক্ষ্য হিসেবে বেছে নেন হোনজো যা রোগ স্থানান্তর সংক্রান্ত ক্যান্সার (Metastatic cancer) নিরাময়ের ক্ষেত্রে কার্যকর। হোনজো এবং এলিসনের পদ্ধতিকে বলা হয় ‘Checkpoint therapy’, যা ক্যান্সার ব্যবস্থাপনা ও নিরাময়ের ক্ষেত্রে কার্যকর। ইতোমধ্যে ফুসফুস ও মূত্রাশয় বা চামড়ার ক্যান্সার নিরাময়ের ক্ষেত্রে এই পদ্ধতির কার্যকারিতা লক্ষ করা গেছে। এই পদ্ধতি এখন অন্যান্য ক্যান্সার নিরাময়ের ক্ষেত্রেও প্রয়োগ করা হচ্ছে।
গত ডিসেম্বরে অনুষ্ঠিত নোবেল পুরস্কার সংক্রান্ত সম্ভোজন বক্তৃতায় (dinner speech) হোনজো উলেস্নখ করেন যে, বিগত অর্ধশতাব্দী ধরে ক্যান্সার আমাদের জীবননাশের এক নম্বর কারণ। মানুষের গড় আয়ু বৃদ্ধি হওয়ার ফলে এই রোগে আক্রান্ত হওয়ার আশঙ্কা বৃদ্ধি পেয়েছে। হোনজো আরো উলেস্নখ করেন যে, অস্ট্রেলিয়ার নোবেল বিজয়ী বিজ্ঞানী স্যার ফ্রাংক মেকফারলেন বার্নেট প্রায় ষাট বছর আগে ক্যান্সার অনাক্রম্য থেরাপির কথা তাত্ত্বিকভাবে প্রস্তাব করেন। তারপর এই পদ্ধতিকে বাস্তবে রূপদানের ক্ষেত্রে অনেকেই কাজ করেছেন, কিন্তু সমর্থ হননি। হোনজো এবং এলিসন পৃথকভাবে আবিষ্কার করেন যে, CTLA-4 এবং PD-1-কে নিয়ন্ত্রণ বা বাধা প্রদানের মাধ্যমে দেহের অনাক্রম্য প্রক্রিয়াকে ত্বরান্বিত করা সম্ভব। এই পদ্ধতি আবিষ্কারের ফলে অনেক ক্যান্সার রোগীকে নিরাময় করা সম্ভব হয়েছে। হোনজোর ভাষায়, ‘We sincerely hope this treatment will reach far and wide so that everybody on our planet can benefit from this evolutionary gift for healthy life.’
সর্বোপরি, লেজার রশ্মি ব্যবহারের নতুন পদ্ধতি, যা চোখের অস্ত্রোপচারসহ চিকিৎসাবিজ্ঞানের অন্যান্য ক্ষেত্রে যুগান্তকারী অবদান রেখে চলেছে, তারই স্বীকৃতি এ-বছর পদার্থবিজ্ঞানে নোবেল পুরস্কার। ডারউইনের বিবর্তনবাদের ধারণাকে কাজে লাগিয়ে ‘নির্দেশিত বিবর্তন পদ্ধতি’ আবিষ্কার এবং জীবাণু ভাইরাস প্রদর্শন পদ্ধতির আবিষ্কার নতুন নতুন পরিবেশবান্ধব রাসায়নিক যৌগ আবিষ্কার এবং চিকিৎসাবিজ্ঞানে যে-যুগান্তকারী অবদান রেখে চলেছে, তারই স্বীকৃতি এ-বছর রসায়নবিজ্ঞানে নোবেল পুরস্কার। ক্যান্সার রোগ নিরাময়ের ক্ষেত্রে মানবদেহের অনাক্রম্য পদ্ধতি প্রয়োগের নতুন পরাকৌশল আবিষ্কার চিকিৎসাবিজ্ঞানে যে যুগান্তকারী অবদান রেখে চলেছে, তারই স্বীকৃতি এ-বছর শারীরবৃত্ত বা চিকিৎসাবিজ্ঞান নোবেল পুরস্কার। এই নোবেল-স্বীকৃত গবেষণা আগামীদিনে মানবকল্যাণে আরো সুফল বয়ে আনবে, তাতে কোনো সন্দেহ নেই।
সহায়ক তথ্যপঞ্জি ও চিত্রঋণ
পদার্থবিজ্ঞান
১. The Royal Swedish Academy of Sciences press release, dated 2 October 2018, on the Nobel Prize in Physics 2018 (Accessed at http://www.nobelprize.org, on 1 Dec. 2018).
২. The Nobel Committee for Physics (2018), Groundbreaking inventions in laser physics (Accessed at http://www.nobelprize.org, on 1 Dec. 2018).
৩. Ashkin, A (1990), Acceleration and Trapping of Particles by Radiation Pressure, Phys. Rev. lett. 24, 156.
৪. Strickland, D and Mourou, G (1985), Compression of amplified chirped optical pulses, optics communications, V 56, No 3, pp 219-221.
রসায়নবিজ্ঞান
১. The Royal Swedish Academy of Sciences press release, dated 3 October 2018, on the Nobel prize in Chemistry 2018 (Accessed at http://www.nobelprize.org, on 2 Dec. 2018).
২. The Nobel Committee for Chemistry Report (2018), Directed evolution of enzymes and binding protins (Accessed at http://www.nobelprize.org, on 2 Dec. 2018).
৩. Smith G. P and Petrenko, V. A (1997), Phage display, Chem. Rev. 97 (2) : 391-410.
৪. Arnold, F. H and Georgian, G (ed), Directed Enzyme Evolution : Screening and Selection Methods, Humana press, N. J (2003).
চিকিৎসাবিজ্ঞান
১. Nobel Assembly at the Karolinska Institute prese release, dated 7 October 2018, on the 2018 Nobel prize in physiology or medicine (Accessed at http://www.nobelprize.org, on 1 Nov. 2018).
২. Edward Smith, G. I, Holmdahl, R, Kaupe, O and Karri, K (2018), Scientific Background : Discovary of Cancer theraphy by inhibition of negative immune regulation, the Nobel Assembly of Karolinska Institute Report.
চিত্রঋণ
এই প্রবন্ধে ব্যবহৃত চিত্র লেখক কর্তৃক ব্যবহারের জন্য দ্য নোবেল ফাউন্ডেশন, স্টকহোম সুইডেন থেকে অনুমোদনপ্রাপ্ত।
চিত্র : ১ (থার্মোফিশার সায়েন্টিফিক)
চিত্র : ২ (নোবেল ফাউন্ডেশন)
চিত্র : ৩ (থার্মোফিশার সায়েন্টিফিক)
চিত্র : ৪ (উইকিপিডিয়া এবং গ্রাহাম বিয়ার্ড)

Leave a Reply
You must be logged in to post a comment.